Hukum Gay-Lussac: Hubungan Tekanan dan Suhu Gas yang Harus Anda Tahu
Oke, berikut adalah draf konten artikel yang dioptimalkan SEO berdasarkan instruksi Anda:
Pernahkah Anda bertanya-tanya mengapa ban mobil bisa meletus saat cuaca panas? Atau mengapa tabung gas LPG harus disimpan di tempat yang sejuk? Jawabannya terletak pada Hukum Gay-Lussac, sebuah prinsip penting dalam termodinamika yang menjelaskan hubungan antara tekanan dan suhu gas pada volume konstan. Mari kita telusuri lebih dalam tentang hukum ini dan aplikasinya dalam kehidupan sehari-hari.
Apa Itu Hukum Gay-Lussac?
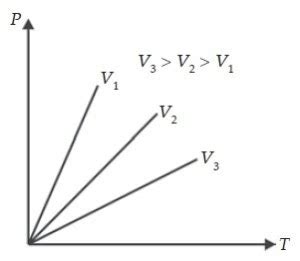
Hukum Gay-Lussac, yang juga dikenal sebagai Hukum Amontons, menyatakan bahwa untuk sejumlah massa gas yang konstan dan pada volume tetap, tekanan gas berbanding lurus dengan suhu absolutnya. Dengan kata lain, jika suhu gas meningkat, maka tekanannya juga akan meningkat, dan sebaliknya. Prinsip ini sangat penting dalam memahami perilaku gas dan penerapannya dalam berbagai teknologi.
Sejarah Singkat Hukum Gay-Lussac
Hukum ini dinamai dari seorang ilmuwan kimia dan fisikawan asal Prancis, Joseph Louis Gay-Lussac, yang mempublikasikan hukum ini pada tahun 1809. Meskipun demikian, Guillaume Amontons, seorang fisikawan Prancis, telah menemukan hubungan ini sebelumnya pada tahun 1702. Oleh karena itu, hukum ini juga sering disebut sebagai Hukum Amontons.
Rumus Hukum Gay-Lussac
Rumus matematis Hukum Gay-Lussac dinyatakan sebagai berikut:
P₁ / T₁ = P₂ / T₂
Dimana:
- P₁ = Tekanan awal gas
- T₁ = Suhu awal gas (dalam Kelvin)
- P₂ = Tekanan akhir gas
- T₂ = Suhu akhir gas (dalam Kelvin)
- Ban Kendaraan: Saat suhu udara meningkat, tekanan udara di dalam ban juga meningkat. Jika tekanan terlalu tinggi, ban bisa meletus.
- Tabung Gas LPG: Tabung gas LPG harus disimpan di tempat yang sejuk untuk menghindari peningkatan tekanan yang berlebihan akibat kenaikan suhu.
- Panci Presto: Panci presto memanfaatkan prinsip Hukum Gay-Lussac untuk meningkatkan suhu didih air dengan meningkatkan tekanan di dalam panci.
- Aerosol: Saat kaleng aerosol dipanaskan, tekanan di dalamnya meningkat, yang dapat menyebabkan ledakan.
- Ubah suhu dari Celsius ke Kelvin:
- Gunakan rumus Hukum Gay-Lussac: P₁ / T₁ = P₂ / T₂
- Masukkan nilai yang diketahui: 200 kPa / 300.15 K = P₂ / 330.15 K
- Selesaikan untuk P₂: P₂ = (200 kPa * 330.15 K) / 300.15 K = 220 kPa
- Apa perbedaan Hukum Gay-Lussac dengan Hukum Boyle?
- Mengapa suhu harus dalam Kelvin saat menggunakan Hukum Gay-Lussac?
- Apakah Hukum Gay-Lussac berlaku untuk semua jenis gas?
Penting: Suhu harus selalu dinyatakan dalam Kelvin (K). Untuk mengkonversi dari Celcius (°C) ke Kelvin (K), gunakan rumus: K = °C + 273.15
Penerapan Hukum Gay-Lussac dalam Kehidupan Sehari-hari
Hukum Gay-Lussac memiliki banyak aplikasi praktis dalam kehidupan sehari-hari. Beberapa contohnya meliputi:
Contoh Soal Hukum Gay-Lussac
Berikut adalah contoh soal yang bisa membantu Anda memahami cara menggunakan Hukum Gay-Lussac:
Sebuah ban mobil memiliki tekanan 200 kPa pada suhu 27°C. Setelah mobil berjalan, suhu ban meningkat menjadi 57°C. Berapakah tekanan ban sekarang?
Penyelesaian:
* T₁ = 27°C + 273.15 = 300.15 K
* T₂ = 57°C + 273.15 = 330.15 K
Jadi, tekanan ban sekarang adalah 220 kPa.
Tips Mengingat Hukum Gay-Lussac
Untuk memudahkan Anda mengingat Hukum Gay-Lussac, ingatlah kata kunci "Tekanan dan Suhu". Hukum ini menekankan hubungan langsung antara kedua variabel tersebut ketika volume gas tetap konstan.
Pertanyaan yang Sering Diajukan (FAQ)
Berikut adalah beberapa pertanyaan umum tentang Hukum Gay-Lussac:
* Hukum Gay-Lussac membahas hubungan antara tekanan dan suhu pada volume konstan, sementara Hukum Boyle membahas hubungan antara tekanan dan volume pada suhu konstan.
* Karena skala Kelvin adalah skala absolut, yang berarti nol Kelvin adalah nol mutlak (keadaan di mana tidak ada energi termal). Menggunakan skala Celsius dapat menghasilkan hasil yang tidak akurat.
* Hukum Gay-Lussac berlaku untuk gas ideal, yaitu gas yang mengikuti asumsi tertentu (misalnya, tidak ada gaya tarik-menarik antar molekul gas). Dalam praktiknya, sebagian besar gas berperilaku mendekati ideal pada kondisi suhu dan tekanan normal.
Kesimpulan
Hukum Gay-Lussac adalah konsep penting dalam termodinamika yang menjelaskan hubungan antara tekanan dan suhu gas pada volume konstan. Memahami hukum ini membantu kita menjelaskan berbagai fenomena di sekitar kita dan menerapkannya dalam teknologi. Dengan memahami prinsip ini, kita bisa lebih berhati-hati dalam menggunakan dan menyimpan benda-benda yang melibatkan gas, seperti ban kendaraan dan tabung LPG.
Semoga artikel ini bermanfaat!